1-INTRODUCTION
L'eau est abondante sur terre, elle représente 1380 millions de km3.
L'essentiel toutefois est constitué d'eau de mer (97,2 %) et de glace
(2,15 %) inutilisables directement. L'eau douce, facilement disponible
(lacs, fleuves, certaines eaux souterraines), ne représente que 0,07 % de
la ressource totale soit environ un million de km3. Mais la répartition de
cette eau est très inégale. En effet, dix pays se partagent 60 % des
réserves d'eau douce et vingt-neuf autres principalement en Afrique et au
Moyen-Orient, sont au contraire confrontés à une pénurie chronique d'eau douce.
Dans ces pays, selon le Water Ressources Institute, 250 millions d'individus,
ne disposent pas aujourd'hui du minimum vital d'eau défini à 1000 m3 par
habitant et par an. 400 millions de personnes vivent en situation de stress
hydrique, estimé entre 1000 et 2000 m3 par habitant et par an. Et on estime que
2,5 milliards de personnes pourraient souffrir du manque d'eau en 2050
compte-tenu de l'évolution de la démographie et de l'augmentation des
consommations d'eau.
Pour faire face à cette pénurie annoncée d'eau, de nouvelles techniques de
production d'eau potable devront être mises en place pour satisfaire les
besoins de la population croissante. Une des techniques prometteuses pour
certains pays est le dessalement de l'eau de mer ou des eaux saumâtres. Les
techniques de dessalement de l'eau de mer sont opérationnelles depuis de
nombreuses années. Mais leur coût (de 1 à 2 euros / m3) limite
souvent leur utilisation aux pays riches ainsi que la disponibilité d’eaux
facilement traitable en terme de germe, pollution et salinité. Cependant au
cours des récentes années, la capacité des usines de dessalement s'est
fortement accrue et les coûts de production par m3 ont connu une forte
diminution grâce aux dernières technologies.
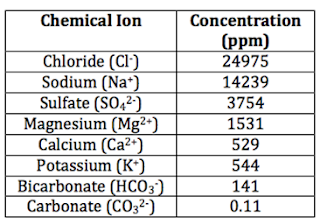
2-COMPOSITION de l'eau de mer
Les océans est
constituée à 96,5 % d'eau pure, le reste se répartissant entre les sels, comme
le chlorure de sodium (notre sel de table) et d'autres éléments chimiques : du
fluor, du soufre, du potassium ou du calcium. Si plus des deux tiers des 94
éléments chimiques naturels sont présents dans l'eau de mer, la plupart le sont
en faible quantité et difficilement décelables.
La caractéristique la
plus importante des eaux de mer est leur salinité, c'est-à-dire leur teneur
globale en sels (chlorures de sodium et de magnésium, sulfates, carbonates). La
salinité moyenne des eaux des mers et océans est de 35 g.L-1
(27,2 g.L-1 de NaCl, 3,8 g.L-1 de MgCl2, 1,7 g.L-1 MgSO4,
1,26 g.L-1 CaSO4, 0,86 g.L-1 K2SO4).
Cette salinité peut être différente dans le cas de mers fermées :
·
Mer Méditerranée : 36 à
39 g.L-1,
·
Mer Rouge : environ 40
g.L-1,
·
Mer Caspienne : 13
g.L-1,
·
Mer Morte : 270 g.L-1,
Sachant que l’eau fraiche dispose de 1500 ppm de total solide dissous
comparée à l’eau de mer qui elle dispose d’entre 10 000 ppm a 45 000
ppm (partie par million).
Le pH moyen des eaux de mer varie entre 7,5 et 8,4 : l'eau de mer est un
milieu légèrement basique.
3-Les principales technologies de
dessalement des eaux
Les technologies actuelles de dessalement des eaux sont classées en
deux catégories, selon le principe appliqué :
·
Les procédés
thermiques faisant intervenir un changement de phases : la congélation et la
distillation.
·
Les procédés
utilisant des membranes : l'osmose inverse et l'électrodialyse.
Parmi les procédés précités, la distillation et l'osmose inverse
sont des technologies dont les performances ont été prouvées pour le
dessalement d'eau de mer. En effet, ces deux procédés sont les plus
commercialisés dans le marché mondial du dessalement. Les autres techniques
n'ont pas connu un essor important dans le domaine à cause de problèmes liés
généralement à la consommation d'énergie et/ou à l'importance des
investissements qu'ils requièrent.
Quel que soit le procédé de séparation du sel et de l'eau envisagé,
toutes les installations de dessalement comportent 4 étapes :
·
Une prise d'eau
de mer avec une pompe et une filtration grossière,
·
Un prétraitement
avec une filtration plus fine, l'addition de composés biocides et de produits
·
Le procédé de
dessalement lui-même,
·
Le
post-traitement avec une éventuelle reminéralisation de l'eau produite.
A l'issue de ces 4 étapes, l'eau de mer est rendue potable ou
utilisable industriellement, elle doit alors contenir moins de 0,5 g de sels
par litre.
a- La
Distillation :
Dans les procédés de distillation, il s'agit de chauffer l'eau de mer pour
en vaporiser une partie. La vapeur ainsi produite ne contient pas de sels, il
suffit alors de condenser cette vapeur pour obtenir de l'eau douce liquide.et
cette méthode est l’un des plus utilisés
tel que elle ont compte a peu prés 60% de l’eau dessalée au monde Il s'agit en
fait d'accélérer le cycle naturel de l'eau. En effet l'eau s'évapore
naturellement des océans, la vapeur s'accumule dans les nuages puis l'eau douce
retombe sur terre par les précipitations. Ce principe de dessalement très
simple a été utilisé dès l'Antiquité pour produire de très faibles quantités
d'eau douce sur les bateaux.
L'inconvénient majeur des procédés de distillation est leur consommation
énergétique importante liée à la chaleur latente de vaporisation de l'eau. En
effet pour transformer un kg d'eau liquide en 1 kg d'eau vapeur à la même
température il faut environ 2250 kilojoules (si le changement d'état se fait à
100°C) . Afin de réduire la consommation d'énergie des procédés industriels,
des procédés multiples effets qui permettent de réutiliser l'énergie libérée
lors de la condensation ont été mis au point.
Deux procédés se partagent le marché du dessalement thermique : le procédé
de distillation à détentes étagées (Multi-Stage Flash distillation
MSF) et le procédé de distillation à multiples effets (Multi-Effect
distillation MED).
b- La
congélation
Différence des
points de congélation de l’eau douce et de l’eau salée
(- 1,9°C pour
une salinité de 35g/l) séparation des cristaux de glace de la saumure, lavage
du sel et fonte
Processus mis
au point aux USA et en Israël.
c- L'ELECTOLYSE
L'électrolyse
est une méthode qui permet de réaliser des réactions chimiques grâce à une
activation électrique. C'est le processus de conversion de l'énergie électrique
en énergie chimique. Elle permet par ailleurs, dans l'industrie chimique, la séparation d'éléments ou la synthèse de composés chimiques. La première
électrolyse par courant continu (électrolyse de l'eau) a été réalisée le 2 mai 1800 par
deux chimistes britanniques, William
Nicholson (1753-1815) et Anthony
Carlisle (1768-1842), quelques
jours après l'invention de la première pile
électrique (publication soumise
le 20 mars 1800 dans une lettre en français au président de la Royal Society, Joseph Banks).
Principe de L'osmose inverse
L'osmose
inverse est un procédé de séparation de l'eau et des sels dissous au moyen de
membranes semi-perméables sous l'action de la pression (54 à 80 bars pour le
traitement de l'eau de mer). Ce procédé fonctionne à température ambiante et
n'implique pas de changement de phase. Les membranes polymères utilisées
laissent passer les molécules d'eau et ne laissent pas passer les particules,
les sels dissous, les molécules organiques de 10-7 mm de taille. L'énergie
requise par l'osmose inverse est uniquement celle électrique consommée
principalement par les pompes haute pression. La teneur en sels de l'eau
osmosée est de l'ordre de de 250 mg/l.
On appelle osmose le transfert de solvant (eau dans la plupart des cas) à
travers une membrane semi-perméable sous l'action d'un gradient de
concentration.
Un système à deux compartiments séparés par une membrane semi-perméable et
contenant deux solutions de concentrations différentes.
Le phénomène d'osmose va se traduire par un écoulement d'eau dirigé de la
solution diluée vers la solution concentrée. Si l'on essaie d'empêcher ce flux
d'eau en appliquant une pression sur la solution concentrée, la quantité d'eau
transférée par osmose va diminuer. Il arrivera un moment où la pression
appliquée sera telle que le flux d'eau s'annulera. Si, pour simplifier, nous supposons
que la solution diluée est de l'eau pure, cette pression d'équilibre est
appelée pression osmotique.
L’eau potable issue de L’osmose inverse passe
par plusieurs étapes de traitement avant d’être distribuer, et parmi ses étapes
on citera :
Abstraction des eaux : L'eau peut être extraite
par les puits côtiers ou Par des systèmes d'admission d'eau de mer tout comme
les puits côtiers et de plage fournissent une eau de meilleure qualité et
Faible teneur en algues et TDS par rapport à l'eau de mer (TDS = solides totaux
dissous)
L’eau s’introduit dans ce qu’on appelle des écrans filaires, une sorte de
tuyau a filtre qui permet de Se débarrasser de certains produits tels les
algues et autres particules Tels que des cailloux.
Prétraitement : Divers contaminants
peuvent endommager la membrane, causant des dommages irréversibles associés à
un rejet réduit et même la destruction de la membrane, de ce fait le prétraitement s’illustrera comme suis
:
Chloration : Le chlore est ajouté à
l'eau brute sous forme de sodium Hypochlorite (NaOCl) ou Chlore gazeux, (Cl2),
et l'eau s’hydrolyse en acide hypochloreux et ce procédé empêche l'encrassement
de la membrane (biologique et Particulaire) et agit comme un désinfectant pour
les bactéries Et autres entités biologiques
Ajustement du PH : ce procédé tant à
ajuster l’acidité de l’eau émanant depuis les sources grâce aux HCl et
H2SO4afin de prévenir la mise à l’échelle de cette dernière qui est due à un
dépassement du niveau de solubilité ainsi une super saturation des Composés
concentré sur le côté source qui se précipite sur la surface de membrane
laissant une couche mince dessus.
Addition de Coagulants et
Floculant :en rajoutant des sels de fer ou d'aluminium (FeCl3, Al2 (SO4)3) a l’eau
,Les solides dissous s'adsorbent sur les hydroxydes formés et Matière
colloïdale à agglomérer qui tentent à se former en masse de ce fait La
sédimentation et la filtration du sable élimine Agrégation naturelle de
minéraux de l'eau de la source.
De-chloration : ce procédé est
l’antagoniste de la chloration puisque il s’agit de ce débarrassé des éléments
chlorique utilisé auparavant et cela avant le processus filtration double
(osmose inverse) afin d’éviter la détérioration de la membrane (polyamides) et
pour cela le métabisulfite de sodium (Na2S2O5) est couramment utilisé.
Filtration double
(osmose-inverse) : l’osmose se
sépare en deux couche à filtre, la première est la membrane asymétrique et la
membrane TFC (thin-film composite) qui fais la particularité du processus et
qui se compose d’une couche très fine de polymère étendu sur un support poreux
en poly sulfone le tout sur un support en soutient de tissu polyester
Désinfection finale de l’eau : la désinfection finale
permettra d’obtenir une eau saine, potable et régulière en minéraux sans aucune
risque sur la santé des consommateurs et ceci grâce a des procédé chimique fin
(fluor, chlore)
4-Avantages et Inconvénients :
Avantages :
Le
dessalement de l'eau de mer et des eaux saumâtres a connu ces dernières années
une avancée remarquable grâce au développement de différents procédés.
Aujourd'hui, plusieurs facteurs militent en faveur de la mise en œuvre de cette
technologie dans notre pays :
-Disponibilité
de l'eau de mer, ressource inépuisable;
-Une
population et une industrie grandes consommatrices d'eau se trouvant à
proximité de la mer;
-Disponibilité
de la ressource énergétique ou combinaison de sa production.
Inconvénients :
-Coût
énergétique encore élevé.
-Rejet
des saumures concentrées au double de la salinité naturelle en mer ou injectées
dans le sol.
-Rejet
d'eaux chaudes en mer dans le cas de la distillation.
-Emploi
de produits chimiques pour nettoyer les membranes (chlore).
-Traces
de cuivre échappés des installations.
-Aucune
législation spécifique concernant la potabilité de l’eau issue de ces
traitements.
5-Procédé économique :
Puis les panneaux solaire thermique ont trouvé leur place ou ont récupère
de l’eau salé qui est chauffé à laide des panneaux solaire thermique, et ont
récupère la vapeur d’eau consoné pour l’utilisé, et le sel récupéré et vendue
pour des industriel.
Et de même pour des industriel qui utilisent le
photo voltaïque sans stockage car il revient plus économique, avec des
ressources énergétique moin pollueuse.
Conclusion :
Le choix du dessalement de l’eau de mer s’est imposé
progressivement dans le monde. En raison du climat, des nombreuses sécheresses
et des besoins de la population grandissants en eau, notamment pour les
cultures, les usages domestiques et le
tourisme, de nombreuses solutions ont été évoquées mais une seule, à savoir le
dessalement de l’eau de mer, a été prise en compte par beaucoup de pays
construit des usines de dessalement qui leur permettent de s’approvisionner en
eau. Dans ce procédé à ce jour, les trois techniques principalement utilisées
pour dessaler l’eau, l’osmose inverse, la distillation et l’électrodialyse
possèdent des avantages certains mais présentent également de nombreuses
contraintes tant économiques qu’écologiques. Ainsi, ces limites amènent des
controverses au niveau scientifique et industriel. Mais des scientifique
recherchent toujours des moyen plus efficaces est plus économique, et à ce jour
l’énergie solaire thermique et solaire photovoltaïque reste la meilleure de ce
point de vue pour avoir une eau douce et préserver l’environnement.
Bibliographie
A. Maurel. Dessalement de l'eau de mer et des
eaux saumâtres et autres procédés non conventionnels d'approvisionnement en eau
douce. Lavoisier Tec&Doc. 2001.
J. Matricon. Vive l'eau. Découvertes
Gallimard. 2000.
P. Danis. Dessalement de l'eau de mer. Techniques
de l'Ingénieur, J 2700. Juin 2003.
Numéro spécial de Science et
Vie sur l'eau, N°211, Juin 2000.
C. Galus, Les techniques de dessalement de l'eau
de mer prennent de l'essor, extrait du Monde, 12 Janvier 2000,
p.24.
Usine Nouvelle,
Septembre 1999.